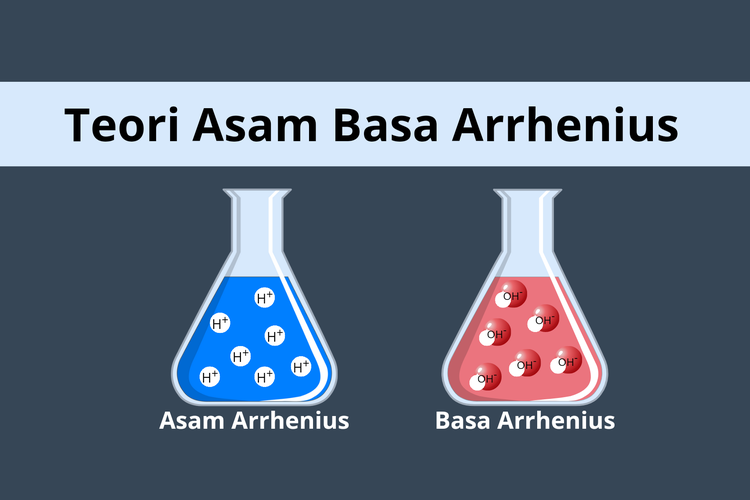
JAKARTA - Setiap hari kita tanpa sadar berinteraksi dengan asam dan basa di sekitar kita. Buah-buahan yang segar memiliki rasa asam, sementara sabun dan detergen memiliki sifat basa yang licin saat disentuh.
Rasa asam pada jeruk berasal dari kandungan H+, sedangkan rasa pahit dan tekstur licin pada sabun muncul karena ion OH-. Fenomena ini menunjukkan bahwa teori asam basa tidak hanya ada di laboratorium, tetapi juga mudah dirasakan dalam kehidupan sehari-hari.
Teori Asam Basa Arrhenius
Kimiawan asal Swedia, Svante Arrhenius, memperkenalkan teori asam basa pertama kali pada tahun 1884. Arrhenius menyatakan bahwa asam adalah senyawa yang menghasilkan ion H+ ketika dilarutkan dalam air.
Asam yang sempurna dalam proses ionisasinya disebut asam kuat, sedangkan asam yang hanya menghasilkan sedikit ion disebut asam lemah. Contohnya, asam sulfat adalah asam kuat, sementara asam asetat termasuk asam lemah.
Sebaliknya, basa menurut Arrhenius adalah zat yang menghasilkan ion OH- ketika dicampur dengan air. Basa kuat menghasilkan banyak ion hidroksida, sedangkan basa lemah hanya menghasilkan sedikit ion OH-.
Namun, teori Arrhenius memiliki keterbatasan karena hanya berlaku pada pelarut air. Basa atau asam yang bekerja di pelarut lain, seperti amonia dalam etanol, tidak termasuk dalam teori ini.
Rumus dan Perhitungan Tingkat Keasaman
Tingkat keasaman atau pH larutan dapat dihitung berdasarkan konsentrasi ion H+. Notasi pH berasal dari p untuk pangkat atau potens dan H untuk atom hidrogen.
Rumus yang digunakan adalah:
pH = -log(H+)
Dengan rumus ini, kita dapat menentukan apakah suatu larutan bersifat asam, netral, atau basa. Larutan dengan pH kurang dari 7 bersifat asam, pH 7 netral, dan pH lebih dari 7 bersifat basa.
Variasi Asam Berdasarkan Jumlah Ion Hidrogen
Teori Arrhenius juga menjelaskan bahwa jumlah ion H+ yang dihasilkan menentukan tipe asam. Asam monoprotik menghasilkan satu H+ per molekul, asam diprotik menghasilkan dua H+, dan asam triprotik menghasilkan tiga H+.
Asam poliprotik adalah asam yang dapat melepaskan lebih dari satu ion H+ per molekul, sehingga memiliki kemampuan untuk menetralkan basa lebih banyak. Contoh asam poliprotik adalah asam fosfat yang menghasilkan tiga ion H+ secara bertahap.
Teori Arrhenius
Teori Arrhenius membantu memahami sifat dasar asam dan basa dalam larutan air. Asam menghasilkan H+, sedangkan basa menghasilkan OH-, dan keduanya dapat digolongkan sebagai kuat atau lemah berdasarkan jumlah ion yang dihasilkan.
Pemahaman teori ini juga mempermudah kita mengenali aplikasi asam dan basa dalam kehidupan sehari-hari. Mulai dari buah-buahan, minuman, hingga produk pembersih, semuanya memiliki sifat kimia yang dapat dijelaskan dengan teori ini.
Dengan mengetahui teori Arrhenius, kita bisa lebih memahami fenomena kimia di sekitar kita. Baik di dapur, laboratorium, maupun saat menggunakan produk rumah tangga, konsep asam dan basa menjadi bagian penting dalam aktivitas sehari-hari.